¿QUE SON?
Las aminas son compuestos químicos orgánicos que se consideran como derivados del amoniaco y resultan de la sustitución de los hidrógenos de la molécula por los radicales alquilo. Según se sustituyan uno, dos o tres hidrógenos, las aminas serán primarias, secundarias o terciarias, respectivamente.
FORMULA GENERAL
| Amoniaco | Amina primaria | Amina secundaria | Amina terciaria |
|---|---|---|---|
 | 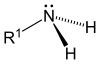 |  | 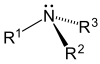 |
ESTRUCTURA DE LA AMINA
PROPIEDADES FÍSICAS
(Constantes físicas de algunas Aminas)
|
PROPIEDADES QUÍMICAS
Las aminas a diferencia del amoniaco arden en presencia de oxígeno por tener átomos de carbono.
Poseen un leve carácter ácido en solución acuosa.
Formación de sales:
Las aminas al ser de carácter básico, son consideradas bases orgánicas. Por lo tanto pueden reaccionar con ácidos para formar sales.
NOMENCLATURA
1. En las aminas sencillas se nombran los radicales unidos al nitrógeno y se termina el nombre con el sufijo amina.
Ejemplos:
- CH3NH2 = metilamina
- CH3-NH-CH3= di-metilamina
CH3 |- N-CH2-CH2-CH3 = Etilmetilpropilamina |CH2-CH3
2. En las aminas mas complejas se prefiere considerar el grupo- NH2 como un sustituyente llamado amino
Ejemplos:
3. Las aminas aromáticas se consideran se consideran derivadas de la anilla.se emplea una N mayúscula para indicar que un grupo alquilico esta unido al nitrógeno y no al anillo aromático.
Ejemplo:
= fenilamina
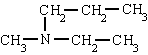 = N-etil-N-metilpropilamina
= N-etil-N-metilpropilaminaCLASIFICACIÓN
Las aminas se clasifican de acuerdo con el número de átomos de hidrógeno del amoniaco que se sustituyen por grupos orgánicos. Las que tienen un solo grupo se llaman aminas primarias, las que tienen dos se llaman aminas secundarias y las que tienen tres, aminas terciarias.
Las aminas sencillas se nombran enumerando los grupos que sustituyen a los átomos de hidrógeno del amoniaco y terminando con amina. Si hay varios grupos o radicales sustituyentes iguales se usan los prefijos di o tri. Cuando se trata de grupos diferentes estos se nombran por orden alfabético (etil antes que metil, o butil antes que propil, prescindiendo del tamaño) y terminando con la terminación amina.
Ejemplos:
| Compuesto | Nombres |
|---|---|
| CH3-NH2 | Metilamina |
| CH3-NH-CH3 | Dimetilamina |
| CH3-CH2-NH-CH2-CH2-CH3 | Etilpropilamina |
| CH3 | N-CH3 | CH3 | Trimetilamina |
| CH3 | N-CH2-CH2-CH3 | CH2-CH3 | Etilmetilpropilamina |
las aminas primarias y secundarias tienen puntos de ebullición menores quelos de los alcoholes, pero mayores que los de los éteres de peso molecularsemejante. Las aminas terciarias, sin puentes de hidrógeno, tienen puntosde ebullición más bajos que las aminas primarias y secundarias de pesos moleculares semejantes.
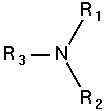
AMINA PRIMARIA : el átomo de nitrógeno (N) lleva un solo grupo R.
AMINA SECUNDARIA: el átomo de nitrógeno (N) llevan dos grupos R
AMINA TERCIARIA: El átomo de nitrógeno (N) llevan tres grupos
¿DONDE SE ENCUENTRAN?
Las aminas como compuestos son muy importantes y reconocidas en industrias como las cosméticas y textiles por el uso o aplicación de la p-Fenilendiamina y algunos derivados se usan en composiciones para teñir el pelo y como antioxidantes para caucho
Las aminas son parte de los alcaloides que son compuestos complejos que se encuentran en las plantas. Algunos de ellos son la morfina y la nicotina. Algunas aminas son biologicamente importantes como la adrenalina y la noradrenalina.
Las aminas secundarias que se encuentran en las carnes y los pescados o en el humo del tabaco.
Estas aminas pueden reaccionar con los nitritos presentes en conservantes empleados en la alimentacion y en plantas, procedentes del uso de fertilizantes, originando N-nitrosoaminas secundarias, que son carcinogenas.
Al degradarse las proteínas se descomponen en distintas aminas, como cadaverina y putrescina entre otras. Las cuales emiten olor desagradable.
Es por ello que cuando la carne de aves, pescado y res no es preservada mediante refrigeración los microorganismos que se encuentran en ella degradan las proteínas en aminas y se produce un olor desagradable.




chevere
ResponderEliminarexelente
ResponderEliminarGracias por la información expuesta, me está ayudando a un trabajo de química 2. Gracias.
ResponderEliminarEste comentario ha sido eliminado por el autor.
ResponderEliminarEsta muy perrona la información ,con esto completo mi exposición de química (8
ResponderEliminarBuena información!!! :D
ResponderEliminarMuy buena información
ResponderEliminarExcelente información,totalmente precisa y fácil de entender
ResponderEliminarBuen trabajo
En la imagen de la estructura de la amina no es la estructura en si de la amina si no de la metilamina, por favor corregir de resto buena información.
ResponderEliminaresta informacion esta muy interesante
ResponderEliminarCómo mítigar el olor de amina líquida
ResponderEliminarQue acido utilizo
Excelente ingormacion , es muy concreta en si 🙃👌
ResponderEliminarque son los grupos R ?
ResponderEliminarson radicales
Eliminarejemplo metil etil propiel butiol etc etc
GRACIAS WEY ME HAZ AYUDADO CON SUBIR LA NOTA DE MI PRUEBA AMEN SI DIOSKERE
ResponderEliminarMUY BUENA INFORMACIÓN
ResponderEliminarGRACIAS ESTA MUY BUENA
ResponderEliminarMuy Buena La Informacion
ResponderEliminarESTA V3RGAS LA INFORMACION.....
ResponderEliminarbuena
ResponderEliminarGracias por la informacion
ResponderEliminarMuy completa y buena la información
ResponderEliminarGracias
Ejemplo de aminas: bencilamina C7H9N, usos...?
ResponderEliminarPungas de información
ResponderEliminarEs una gran información
ResponderEliminarMuy bueno
ResponderEliminarLa siguiente reacción CH3-COOH+NH3 que resultado da
ResponderEliminarVale verga la puta escuelaaaaaaaaa... que chingue a toda su perra madre el profe vergueado viejillo de quimica
ResponderEliminarcalla puta
Eliminartal vez lo dices por que tu no sabes nada y eres un fracasado de mierda das asco con lo que dices seguro eres el ultimo del salon
EliminarQuisiera saber sobre la amina terciaria relacionado con los desinfectantes cuales son
ResponderEliminartu estas de acuedo con el que respondio el 27 de noviembre de 2019
Eliminara que se obedece que las primeras ánimas sean gaseosas hasta el carbono 11, líquidas y del 12 se componen sólidas
ResponderEliminarmuy bueno
ResponderEliminarRe buena esta pagina xdxd
ResponderEliminarMe encanto
ResponderEliminarLa buena pai
ResponderEliminar